近日,由甘肃省食品药品监督管理局主办,省药品医疗器械安全监测与评价中心承办的新修订的《药品不良反应报告和监测管理办法》培训班在兰州市举办。全省14个市州和甘肃矿区食品药品监督管理局及药品生产企业、医疗机构药品不良反应监测人员参加培训。
开班式上,甘肃省食品药品监督管理局负责人指出,通过几年的努力,全省药品不良反应报告和监测工作取得了可喜的成绩,新办法的颁布实施,对做好药品安全监测工作是一个很好的机遇,也给监测与评价工作提出了新的、更高的要求。各级食品药品监管部门要充分认识做好药品安全性监测工作的重要性和必要性,进一步增强责任感和紧迫感。各级监测部门要切实加强机构建设,不断提高监测能力和水平。药品生产、经营企业和医疗机构要加强药品不良反应监测工作,按照《办法》要求,切实履行职责,为保障公众用药安全做出贡献。
培训班邀请了国家药品不良反应监测中心及省内外从事药品不良反应监测的专家授课,分别从《药品不良反应报告和监测管理办法》修订要点,《药品不良反应报告和监测管理办法》条文释义,药品生产企业在不良反应监测中的责任,定期安全性更新报告撰写规范,死亡病例、群体事件的报告与处置,医疗机构如何做好药品不良反应监测工作,药品不良反应报告表填写要求及示例等7个方面进行了全面的讲解。
经过培训,提高了参训人员对新《办法》的认识与理解,明确了相关的工作流程和要求,充实了监测业务知识,为推动全省药品不良反应监测工作的进一步发展奠定了良好基础。
(责任编辑:晏霏霏)
39健康网(www.39.net)专稿,未经书面授权请勿转载。

 39健康网
39健康网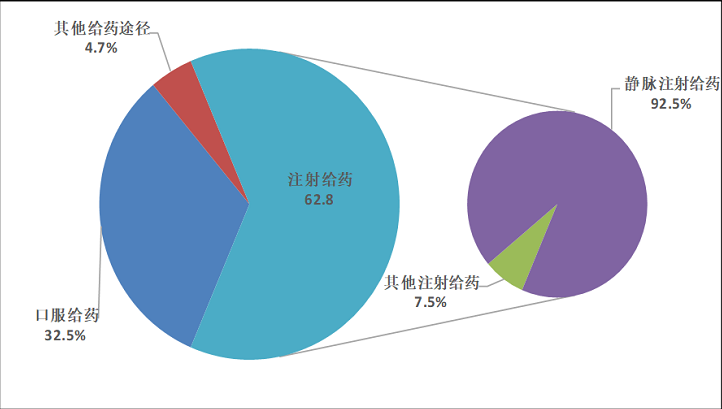 注射给药占药品不良反应的62.8% 输液回血、输入空气会不会致命?
注射给药占药品不良反应的62.8% 输液回血、输入空气会不会致命? 长期服药竟致老年人跌倒?
长期服药竟致老年人跌倒? 识别药品不良反应 消费者勿“中招”
识别药品不良反应 消费者勿“中招” 药品不良反应报告:家中常备成“谨慎用药”
药品不良反应报告:家中常备成“谨慎用药” 药品风险不能警示了之
药品风险不能警示了之 安乃近滴鼻液等7个品种被注销,它有严重副作用!
安乃近滴鼻液等7个品种被注销,它有严重副作用! 食药总局:将对独一味口服制剂说明书进行修订
食药总局:将对独一味口服制剂说明书进行修订 山西发放万余册药品不良反应科普丛书
山西发放万余册药品不良反应科普丛书 “种植一口牙相当县城买套房” 种植牙集采要来了 能降多少?
“种植一口牙相当县城买套房” 种植牙集采要来了 能降多少? 想想都痛!女子健身房上私教课腿骨被压折,如何避免运动中受到伤害?
想想都痛!女子健身房上私教课腿骨被压折,如何避免运动中受到伤害? 武汉大学一例霍乱病例情况,霍乱是什么病?
武汉大学一例霍乱病例情况,霍乱是什么病? 还有这等好事?研究发现多照镜子或有助减肥!
还有这等好事?研究发现多照镜子或有助减肥!
























